文/陳韻涵輯
美國國立衛生研究院(NIH)「腦科學計畫」(BRAIN Initiative)領導的聯合研究10月上旬陸續在三大權威期刊上發表共21篇開創性論文,揭示科學界對大腦理解的重大成果,比較人類和靈長類動物大腦複雜細胞的組成差異,利用創新的「單細胞轉錄組學」,研究人員得以辨識出比先前認知多10倍的3000多種不同腦細胞及其獨特功能。
這21篇論文分別刊登於《科學》(Science,12篇)、《科學進展》(Science Advances,8篇),以及《科學轉化醫學》(Science Translational Medicine,1篇),涵蓋廣泛的研究主題,鑽研人類大腦的獨特性,提供前所未有的人類大腦詳盡組織圖譜。
這批研究考察、分析與對照人類和其他靈長類動物,如黑猩猩、大猩猩、恆河猴和狨猴大腦之間的相似性和差異,說明人類脫離親近屬性的靈長類動物,並真正演化成為人類的關鍵因素。
●近1000億個神經元 組成大腦
人腦的功能非常複雜,可分為粗略感知、移動、閱讀、寫作、說話和思考等,大腦細胞的組成也相當多元。
被稱作「神經元」(Neurons)的神經細胞是大腦的基本單位,用以接收感覺,將指令傳到肌肉,並沿途傳遞電子訊號。
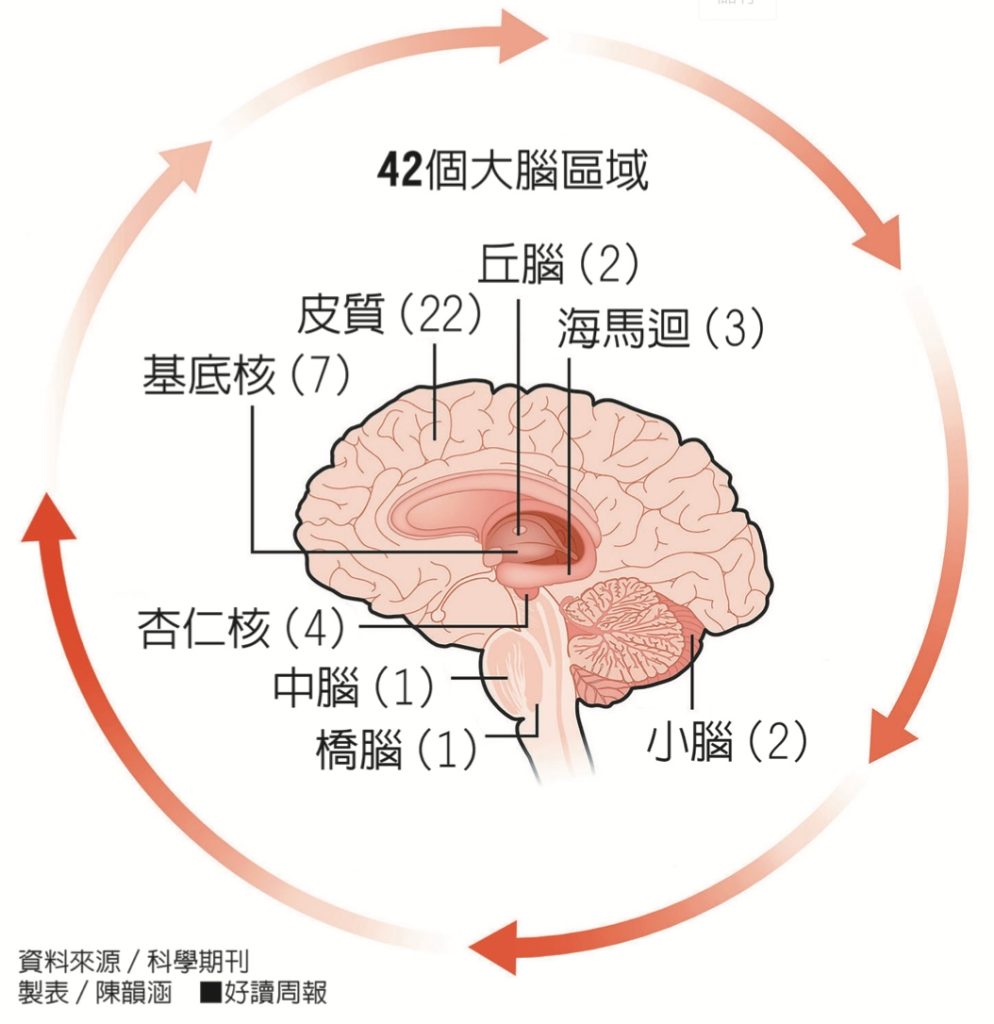
大腦由將近1000億個「神經元」和更多的「非神經元」細胞組成,這些細胞由數百個不同的大腦結構組成,而這些結構管控一系列功能。
相關研究辨識出超過3000種腦細胞類型,此數量約是先前已知腦細胞類型的10倍,並為每一種細胞類型建置完整的基因集(gene set,指一群基因的集合),同時繪製各種細胞與基因集在大腦中的區域分布圖。
●不同細胞不同特性 影響不同
參與研究的美國西雅圖「艾倫腦科學研究所」神經科學家雷恩(Ed Lein)表示:「腦細胞圖譜為我們身而為人所能做的一切,提供了小至細胞層面的詳盡基礎。」雷恩表示,不同的細胞類型具有不同特性,且可能對疾病造成不同影響。
●多樣性集中成熟區 非新皮質
研究成果令學者訝異的是,細胞多樣性大多集中在大腦進化較成熟的部分,即中腦與後腦,而不是負責學習、決策、感官知覺、記憶和語言等更高認知功能的「新皮質」(neocortex)。
對科學家而言,目前最棘手的大腦疾病包括阿茲海默症(Alzheimer’s)、帕金森氏症(Parkinson’s),以及肌萎縮性脊髓側索硬化症(Amyotrophic lateral sclerosis,簡稱ALS)。
ALS是「運動神經元疾病」(motor neuron diseases)的其中一類,這種俗稱「漸凍症」的疾病幾年前因為慈善活動「冰桶挑戰」而廣為人知,是指因運動神經元漸進性退化而造成全身肌肉萎縮及無力的疾病。
漸凍症可依退化部位和好發年齡,分為:
①好發於中老年人、上/下運動神經元都退化的「肌萎縮性脊髓側索硬化症」(ALS)。
②好發於中老年人、上運動神經元退化的「原發性脊髓側索硬化症」(PLS)。
③好發於成人、下運動神經元退化的「漸進性肌肉萎縮症」(PMA)。
④好發於40歲以上病患、下運動神經元退化的「甘迺迪氏症」(Kennedy Disease)。
●圖譜可當研究基準 理解疾病
雷恩表示:「大多數腦部疾病目前仍然缺乏有效的治療方法或無法根治,而腦細胞圖譜可作為未來研究的基準,加速我們理解大腦疾病的詳盡細胞背景,並研發下一代的治療方法。」
研究人員繪製了與阿茲海默症以及精神分裂症、躁狂抑鬱症和重度憂鬱症等各種精神疾病相關的基因「開關」與腦細胞類型,證實大腦中的免疫細胞「小膠質細胞」(microglia cells)與阿茲海默症之間的關聯,並發現某些類型的大腦神經元與精神分裂症息息相關。精神分裂症(schizophrenia)是一種與現實脫節的精神重症。
●特定細胞分子修飾 人腦與眾不同關鍵
這項大規模研究由美國國立衛生研究院的「腦科學計畫」統籌與贊助,相關科學研究工作涉及全球45個機構超過250名科學家,旨在探索和編目靈長類動物(包括人類)的大腦複雜細胞組成。
研究人員透過比較人類,以及人類在演化上的黑猩猩(chimpanzee)和大猩猩(gorilla)等猿類「近親」的顳葉皮質(temporal cortex),探查人類獨特的大腦特徵。
顳葉皮質是大腦中,攸關語言理解及其他高階認知功能的新皮質區域,研究這個區塊可洞悉靈長類動物共有的細胞結構,以及神經元連接和迴路結構的基因差異。
儘管細胞組織相似,特定基因在人類大腦中的利用方式,與黑猩猩和大猩猩不同,其中包括許多涉及神經元連接的基因。
艾倫研究所的神經科學家巴肯(Trygve Bakken)解釋:「這表示人類皮質神經元加速『特化』,這可能導致皮質迴路功能和人類獨特認知功能的差異。」特化(specialization)指的是生物從「一般」演進為「特殊」的方式與過程。
雷恩補充說道,比起黑猩猩和大猩猩,人類特定細胞類型發生分子修飾(molecular modification),可能影響這些細胞「如何連接及其串接可塑性,且可能是人腦與眾不同的關鍵」。